
中科院化学所汪铭团队实现活体动物蛋白质精准降解清除
1月17日,中新网于北京发布了一则消息,记者是孙自法,该消息指出,在复杂生命体系里,怎样精准地清除“致病蛋白”,这属于化学生物学以及生命科学研究面临的一个核心挑战 。
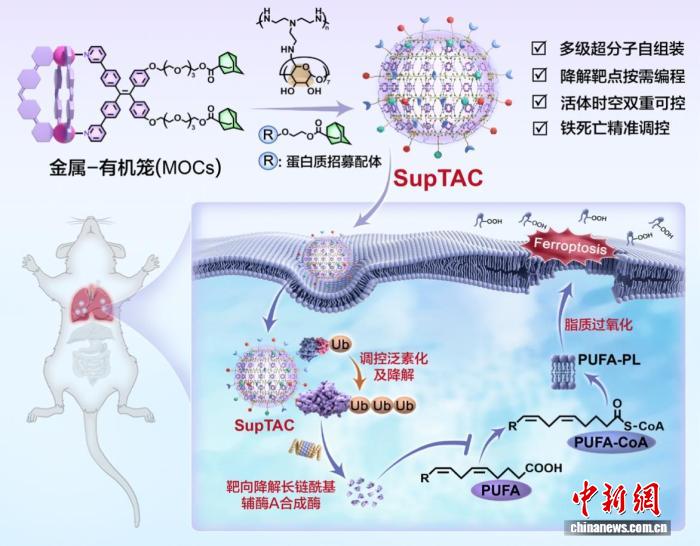
本项有着超分子靶向嵌合体的研究,意图实现时空可控的活体白质降解,由中国科学院化学研究所供图 。
中国科学院化学研究所传来最新消息,汪铭研究团队经创新构建超分子靶向嵌合体,也就是SupTAC,首次于活体动物水平达成 programmable、时空可控的蛋白质精准降解以及清除,进而为蛋白质稳态调控与疾病治疗研究开拓了新路径。
论文是关于这项基础研究的重要研究成果,该成果相关服务健康应用,在北京时间1月17日凌晨,于国际学术期刊《细胞》(Cell)上线发表 。
论文通讯作者,是汪铭研究员,其介绍称,靶向蛋白质降解技术,是通过调控靶蛋白的泛素化,并且经由细胞内天然的蛋白酶体系统来进行降解的,这为“致病蛋白”的选择性清除,提供了全新的策略。然而,现有蛋白质降解技术,在体内应用的时候,往往很难同时兼顾蛋白质降解的时间选择性,以及空间组织选择性,进而导致降解效率降低,并且面临脱靶风险。

在实验室里,有着论文通讯作者汪铭(位于右侧),还有论文第一作者刘计,此图片由中国科学院化学研究所提供,有标点符号。
在这项研究里头,研究团队把超子化学这前沿理念跟蛋白质化学生物学前沿理念创新融合一块儿,借助金属 - 有机笼多级自组装技术制出超分子纳米粒,这纳米粒结构稳定,表面还能功能化。基于此状况,研究团队在纳米粒表面原位组装靶蛋白招募配体,还组装E3泛素连接酶招募配体,成功构建起超分子靶向嵌合体,达成了对靶蛋白泛素化修饰和降解的精准调控。
有着可编程特性的超分子靶向嵌合体,能通过更换不同的靶蛋白招募配体,达成多种蛋白质的协同降解,拥有灵活适配清除多样致病蛋白需求的能力。超分子靶向嵌合体还具备空间组织选择性,可通过调控其表面物理化学性质以及在体内的受体识别作用,构建肺、肝等特定组织中靶蛋白的降解办法,还成功达成了肺部长链酰基辅酶A合成酶的靶向降解,显著抑制了脂多糖所诱导的肺细胞铁死亡以及炎症反应。

进行本项研究的,是中国科学院化学研究所的汪铭研究团队。他们有一张合影,由中国科学院化学研究所提供图片 。
研究团队进一步借助引入生物正交激活策略,来对蛋白质招募配体开展“锁定 - 激活”化学设计,通过外源小分子触发超分子靶向嵌合体原位激活,进而实现特定时间窗口内的蛋白质精准降解,以此解决了传统技术难以精准控制蛋白质降解时机这项难题,研究显示,超分子靶向嵌合体在涵盖非人灵长类动物的多种模型里均展现出稳定、高效的时空可控蛋白质降解性能。
汪铭表达看法称,超分子靶向嵌合体冲破了传统靶向蛋白降解技术的时空调控界限,搭建起细胞以及活体内蛋白质定时、定点开展降解的研究平台 ,此项成果深度汇集中超分子化学与化学生物学的交叉优势,不但为复杂生命体系里蛋白质稳态调控赐予了全新策略,还于疾病机制解析之中、创新药物靶点发现等领域彰显出巨大应用潜藏能力,有希望促使靶向蛋白质降解技术朝临床转化迈进关键一步 。
作者:编辑